Hauptinhalt
Topinformationen
Pressemeldung
Nr. 35 / 2020
07. Februar 2020 : Wie kommunizieren Zellen bei der Blutbildung? Wissenschaftler entdecken, wie fehlgeleitete Kommunikation zwischen Zellen zu Leukämie führt
Wie vermitteln Botenstoffe die Entwicklung neuer Blutzellen und wie geraten diese Prozesse bei Leukämie-Erkrankungen außer Kontrolle? In Kooperation mit Wissenschaftlern aus Großbritannien, Finnland und den USA konnte der Biophysiker Prof. Dr. Jacob Piehler vom Fachbereich Biologie/ Chemie der Universität Osnabrück den zugrundeliegenden molekularen Mechanismus jetzt aufklären. Die Ergebnisse dieses Forschungsprojekts stellen sie in einem Artikel in der renommierten Fachzeitschrift „Science“ (https://science.sciencemag.org/content/367/6478/643) vor, der am 7. Februar erschienen ist.
Zum Hintergrund: Bei einem erwachsenen Menschen werden täglich Milliarden reifer Blutzellen gebildet. Die Entwicklung und Vermehrung der verschiedenen Zelltypen des Bluts aus blutbildenden Stammzellen im Knochenmark wird durch Botenstoffe der Familie der Zytokine kontrolliert. Diese binden an Rezeptoren auf der Oberfläche von Vorläufer-Zellen. Dadurch werden Signalkaskaden aktiviert, die sowohl Wachstum und Zellteilung als auch die Ausdifferenzierung in verschieden Zelltypen steigern. Verschiedene Leukämie-Erkrankungen werden mit genetischen Mutationen in Verbindung gebracht, bei denen diese Signalwege auch ohne Botenstoffe, also unkontrolliert, aktiviert sind. Bislang war es unklar, wie einzelne Mutationen diese Signalaktivierung auf molekularer Ebene auslösen und damit zu diesen schwerwiegenden Erkrankungen des blutbildenden Systems führen.
Erstautor Dr. Stephan Wilmes, der das Projekt als Postdoktorand an der Universität Osnabrück begonnen hatte, berichtet: „Es war wirklich inspirierend, diese spannende biomedizinische Fragestellung mit neuen biophysikalischen Methoden anzugehen, die ich hier während meiner Doktorarbeit entwickelt hatte.“ „Eine besondere Herausforderung dabei war es, die verschiedenen Forschungsansätze der beteiligten Arbeitsgruppen zu koordinieren“, so Maximillian Hafer, der inzwischen die Projektverantwortung übernommen hat.
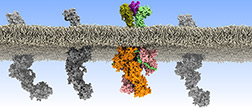
Durch Einzelmolekülmikroskopie an lebenden Zellen konnten die Forscher jetzt erstmals eindeutig nachweisen, dass die Rezeptoren durch die Botenstoffe zur Paaren verbunden werden. Bislang wurde angenommen, dass die Rezeptoren auch ohne Botenstoff bereits als inaktive Paare vorliegen. Aus ihren neuen Beobachtungen an höchstauflösenden Fluoreszenzmikroskopen schlossen die Forscher hingegen, dass die Paarbildung selbst der grundlegende Schalter zur Aktivierung der Signalvermittlung in der Zelle ist.
„Durch die direkte mikroskopische Visualisierung einzelner Rezeptoren unter physiologischen Bedingungen konnten wir eine Kontroverse klären, die dieses Forschungsgebiet seit mehr als 20 Jahren beschäftigt“, erklärt Prof. Dr. Jacob Piehler.
Durch Kombination mit biomedizinischen Untersuchungen an den Universitäten York und Dundee fanden die Forscher heraus, dass viele krankheitsrelevante Mutationen bereits ohne Botenstoff zur Paarbildung bestimmter Rezeptoren führten. „Diese Beobachtungen brachten uns auf die Spur eines bislang unbekannten Mechanismus, wie einzelne Mutationen an diesem Rezeptor zu Leukämie-Erkrankungen führen“, erläutert Prof. Ian Hitchcock von der Universität York.
Kooperationspartner an der Universität Helsinki nutzten diese Ergebnisse, um über Simulationsrechnungen und molekulare Modellierung ein vollständiges Strukturmodell auf atomarer Skala zu entwickeln, das die unterschiedlichen Wirkungsweisen verschiedener Mutationen erklären konnte. „Unsere Strukturmodelle zeigten außerdem überraschende Effekte in Hinblick auf die Ausrichtung der aktiven Rezeptorpaare an der Zellmembran. Diese Vorhersagen konnten anschließend experimentell bestätigt werden“, erklärt Prof. Ilpo Vattulainen von der Universität Helsinki.
Diese grundlegenden Einsichten in die Funktionsweise von Rezeptoren ermöglichen nicht nur völlig neue und wesentlich gezieltere Strategien für die Bekämpfung von Leukämie-Erkrankungen. Darüber hinaus vermuten die Forscher, dass sich eine ganze Reihe von entzündlichen und allergischen Erkrankungen ebenfalls auf ähnliche Mechanismen zurückführen lassen.
Der Artikel in der Fachzeitschrift „Science“ ist abrufbar unter: https://science.sciencemag.org/content/367/6478/643
Weitere Informationen für die Redaktionen:
Prof. Dr. Jacob Piehler, Universität Osnabrück
Fachbereich Biologie/ Chemie & Center of Cellular Nanoanalytics (CellNanOs)
Barbarastraße 11, 49076 Osnabrück
Tel.: +49 541 969 2800
piehler@uos.de